Пептиди су класа једињења која се формирају повезивањем више аминокиселина преко пептидних веза.Они су свеприсутни у живим организмима.До сада су десетине хиљада пептида пронађене у живим организмима.Пептиди играју важну улогу у регулисању функционалних активности различитих система, органа, ткива и ћелија иу животним активностима, а често се користе у функционалној анализи, истраживању антитела, развоју лекова и другим пољима.Са развојем биотехнологије и технологије синтезе пептида, све више и више пептидних лекова се развија и примењује у клиници.
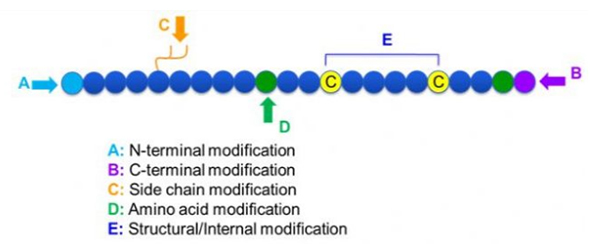
Постоји широк спектар модификација пептида, које се једноставно могу поделити на пост модификацију и модификацију процеса (користећи модификацију изведених амино киселина), и модификацију Н-терминала, модификацију Ц-терминала, модификацију бочног ланца, модификацију аминокиселина, модификацију скелета, итд., у зависности од места модификације (слика 1).Као важно средство за промену структуре главног ланца или група бочних ланаца пептидних ланаца, модификација пептида може ефикасно променити физичка и хемијска својства пептидних једињења, повећати растворљивост у води, продужити време деловања ин виво, променити њихову биолошку дистрибуцију, елиминисати имуногеност. У овом раду представљено је неколико главних стратегија модификације пептида и њихове карактеристике.
1. Циклизација
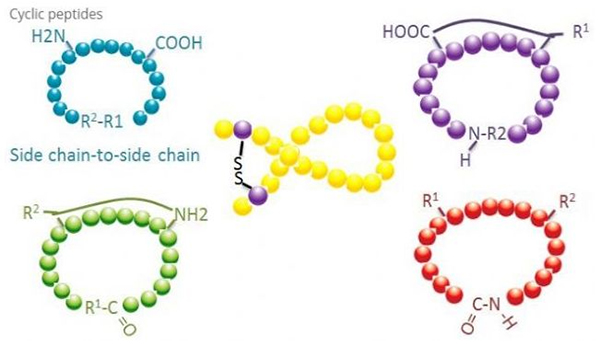
Циклични пептиди имају многе примене у биомедицини, а многи природни пептиди са биолошком активношћу су циклични пептиди.Пошто циклични пептиди имају тенденцију да буду ригиднији од линеарних пептида, они су изузетно отпорни на дигестивни систем, могу да преживе у дигестивном тракту и показују јачи афинитет за циљне рецепторе.Циклизација је најдиректнији начин за синтезу цикличних пептида, посебно за пептиде са великим структурним скелетом.Према начину циклизације, може се поделити на тип бочног ланца, тип бочног ланца, тип терминала - тип терминала (тип с краја на крај).
(1) сидецхаин-то-сидецхаин
Најчешћи тип циклизације бочног ланца у бочни ланац је дисулфидно премошћавање између остатака цистеина.Ова циклизација је уведена тако што се пар цистеинских остатака депротектира и затим оксидује да би се формирале дисулфидне везе.Полициклична синтеза се може постићи селективним уклањањем сулфхидрилних заштитних група.Циклизација се може обавити или у растварачу након дисоцијације или на смоли пре дисоцијације.Цицлизација на смолама може бити мање ефикасна од циклизације растварача јер пептиди на смолама не формирају лако циклификоване конформације.Други тип циклизације бочног ланца - бочног ланца је формирање амидне структуре између остатка аспарагинске киселине или глутаминске киселине и базне амино киселине, што захтева да заштитна група бочног ланца мора бити у стању да се селективно уклони из полипептида или на смоли или после дисоцијације.Трећи тип циклизације бочног ланца - бочног ланца је формирање дифенил етера помоћу тирозина или п-хидроксифенилглицина.Ова врста циклизације у природним производима налази се само у микробним производима, а производи циклизације често имају потенцијалну медицинску вредност.Припрема ових једињења захтева јединствене реакционе услове, тако да се не користе често у синтези конвенционалних пептида.
(2) терминал-бочни ланац
Циклизација крајњег ланца обично укључује Ц-терминал са амино групом бочног ланца лизина или орнитина, или Н-терминал са бочним ланцем аспарагинске киселине или глутаминске киселине.Друга циклизација полипептида се врши формирањем етарских веза између терминала Ц и бочних ланаца серина или треонина.
(3) Тип терминала или типа од главе до репа
Полипептиди ланца могу се или циклирати у растварачу или фиксирати на смолу циклирањем бочног ланца.Ниске концентрације пептида треба да се користе у централизацији растварача да би се избегла олигомеризација пептида.Принос синтетичког прстенастог полипептида од главе до репа зависи од секвенце полипептида ланца.Стога, пре припреме цикличних пептида у великој мери, прво треба креирати библиотеку могућих ланчаних оловних пептида, након чега следи циклизација да би се пронашла секвенца са најбољим резултатима.
2. Н-метилација
Н-метилација се првобитно јавља у природним пептидима и уводи се у синтезу пептида да би се спречило стварање водоничних веза, чиме се пептиди чине отпорнијим на биоразградњу и клиренс.Синтеза пептида коришћењем Н-метилованих деривата аминокиселина је најважнији метод.Поред тога, може се користити и Митсунобу реакција интермедијара полипептида-смоле Н-(2-нитробензен сулфонил хлорид) са метанолом.Овај метод је коришћен за припрему библиотека цикличних пептида које садрже Н-метиловане аминокиселине.
3. Фосфорилација
Фосфорилација је једна од најчешћих посттранслационих модификација у природи.У људским ћелијама више од 30% протеина је фосфорилисано.Фосфорилација, посебно реверзибилна фосфорилација, игра важну улогу у контроли многих ћелијских процеса, као што су трансдукција сигнала, експресија гена, регулација ћелијског циклуса и цитоскелета и апоптоза.
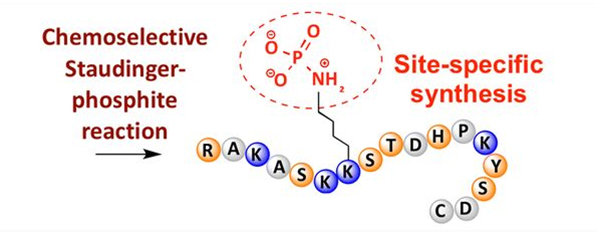
Фосфорилација се може приметити на различитим остацима аминокиселина, али најчешћи циљеви фосфорилације су остаци серина, треонина и тирозина.Деривати фосфотирозина, фосфотреонина и фосфосерина могу се или увести у пептиде током синтезе или формирати након синтезе пептида.Селективна фосфорилација се може постићи коришћењем остатака серина, треонина и тирозина који селективно уклањају заштитне групе.Неки реагенси за фосфорилацију такође могу да уведу групе фосфорне киселине у полипептид накнадном модификацијом.Последњих година, фосфорилација лизина специфична за место је постигнута коришћењем хемијски селективне Стаудингер-фосфитне реакције (слика 3).
4. Миристоилација и палмитоилација
Ацилација Н-терминала са масним киселинама омогућава пептидима или протеинима да се вежу за ћелијске мембране.Миридамоилирана секвенца на Н-терминалу омогућава да протеин киназе породице Срц и Гак протеини реверзне транскриптазе буду циљани да се вежу за ћелијске мембране.Миристинска киселина је везана за Н-терминал смоле-полипептида коришћењем стандардних реакција купловања, а резултујући липопептид је могао да се дисоцира под стандардним условима и пречисти помоћу РП-ХПЛЦ.
5. Гликозилација
Гликопептиди као што су ванкомицин и теиколанин су важни антибиотици за лечење бактеријских инфекција отпорних на лекове, а други гликопептиди се често користе за стимулацију имуног система.Поред тога, пошто су многи микробни антигени гликозиловани, од великог је значаја проучавање гликопептида за побољшање терапеутског ефекта инфекције.С друге стране, откривено је да протеини на ћелијској мембрани туморских ћелија показују абнормалну гликозилацију, због чега гликопептиди играју важну улогу у истраживању рака и имунолошке одбране тумора.Гликопептиди се припремају Фмоц/т-Бу методом.Гликозиловани остаци, као што су треонин и серин, се често уводе у полипептиде помоћу фМОЦ активираних пентафлуорофенол естаром да би се заштитиле гликозиловане аминокиселине.
6. Изопрен
Изопентадиенилација се дешава на остацима цистеина у бочном ланцу близу Ц-терминала.Протеин изопрен може побољшати афинитет ћелијске мембране и формирати интеракцију протеин-протеин.Изопентадијеновани протеини укључују тирозин фосфатазу, малу ГТазу, молекуле кохаперона, нуклеарну ламину и центромерне везујуће протеине.Изопрен полипептиди се могу припремити коришћењем изопрена на смолама или увођењем деривата цистеина.
7. Модификација полиетилен гликола (ПЕГ).
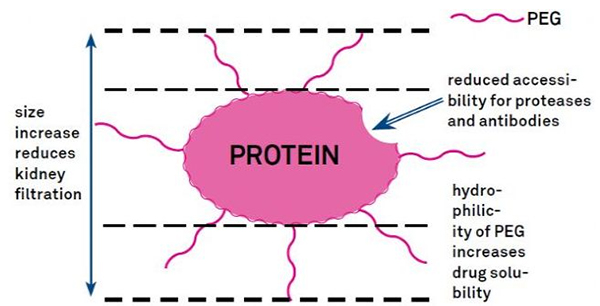
ПЕГ модификација се може користити за побољшање хидролитичке стабилности протеина, биодистрибуције и растворљивости пептида.Увођење ПЕГ ланаца у пептиде може побољшати њихова фармаколошка својства и такође инхибирати хидролизу пептида помоћу протеолитичких ензима.ПЕГ пептиди пролазе кроз попречни пресек гломеруларне капиларе лакше од обичних пептида, значајно смањујући бубрежни клиренс.Због продуженог активног полуживота ПЕГ пептида ин виво, нормалан ниво третмана се може одржавати нижим дозама и ређим пептидним лековима.Међутим, ПЕГ модификација такође има негативне ефекте.Велике количине ПЕГ спречавају ензим да разгради пептид и такође смањују везивање пептида за циљни рецептор.Али низак афинитет ПЕГ пептида је обично надокнађен њиховим дужим фармакокинетичким полуживотом, а будући да су присутни у телу дуже, ПЕГ пептиди имају већу вероватноћу да се апсорбују у циљна ткива.Због тога спецификације ПЕГ полимера треба оптимизовати за оптималне резултате.С друге стране, ПЕГ пептиди се акумулирају у јетри због смањеног бубрежног клиренса, што доводи до макромолекуларног синдрома.Стога, модификације ПЕГ-а морају бити дизајниране пажљивије када се пептиди користе за тестирање лекова.
Уобичајене модификационе групе ПЕГ модификатора могу се грубо сумирати на следећи начин: Амино (-амин) -НХ2, аминометил-Цх2-НХ2, хидрокси-ОХ, карбокси-Цоох, сулфхидрил (-Тиол) -СХ, Малеимид -МАЛ, сукцинимид карбонат - СЦ, сукцинимид ацетат -СЦМ, сукцинимид пропионат -СПА, н-хидроксисукцинимид -НХС, акрилат-цх2цх2цоох, алдехид -ЦХО (као што је пропионал-алд, бутирАЛД), акрилна база (-акрилат-ацрл, азидо-азид) Биотин, флуоресцеин, глутарил -ГА, акрилат хидразид, алкин-алкин, п-толуенсулфонат -ОТс, сукцинимид сукцинат -СС, итд. Деривати ПЕГ-а са карбоксилним киселинама могу бити купловани за н-терминалне амине или бочне ланце лизина.Амино-активирани ПЕГ може бити спојен на бочне ланце аспарагинске киселине или глутаминске киселине.Мал-активирани ПЕГ се може коњуговати са меркаптаном потпуно депротектованих бочних ланаца цистеина [11].ПЕГ модификатори се обично класификују на следећи начин (напомена: мПЕГ је метокси-ПЕГ, ЦХ3О-(ЦХ2ЦХ2О)н-ЦХ2ЦХ2-ОХ):
(1) ПЕГ модификатор равног ланца
мПЕГ-СЦ, мПЕГ-СЦМ, мПЕГ-СПА, мПЕГ-ОТс, мПЕГ-СХ, мПЕГ-АЛД, мПЕГ-бутирАЛД, мПЕГ-СС
(2) бифункционални ПЕГ модификатор
ХЦОО-ПЕГ-ЦООХ, НХ2-ПЕГ-НХ2, ОХ-ПЕГ-ЦООХ, ОХ-ПЕГ-НХ2, ХЦл·НХ2-ПЕГ-ЦООХ, МАЛ-ПЕГ-НХС
(3) модификатор ПЕГ гранања
(мПЕГ)2-НХС, (мПЕГ)2-АЛД, (мПЕГ)2-НХ2, (мПЕГ)2-МАЛ
8. Биотинизација
Биотин може бити снажно везан са авидином или стрептавидином, а снага везивања је чак близу ковалентне везе.Биотином обележени пептиди се обично користе у имуноесејима, хистоцитохемији и проточној цитометрији заснованој на флуоресценцији.Обележена антибиотска антитела се такође могу користити за везивање биотинилованих пептида.Ознаке биотина су често везане за бочни ланац лизина или Н терминал.6-аминокапроична киселина се често користи као веза између пептида и биотина.Веза је флексибилна у везивању за подлогу и боље се везује у присуству стеричних препрека.
9. Флуоресцентно обележавање
Флуоресцентно обележавање се може користити за праћење полипептида у живим ћелијама и за проучавање ензима и механизама деловања.Триптофан (Трп) је флуоресцентан, тако да се може користити за интринзично обележавање.Спектар емисије триптофана зависи од периферног окружења и смањује се са смањењем поларитета растварача, што је особина која је корисна за откривање структуре пептида и везивања рецептора.Флуоресценција триптофана се може угасити протонираном аспарагинском киселином и глутаминском киселином, што може ограничити његову употребу.Дансил хлоридна група (Дансил) је високо флуоресцентна када је везана за амино групу и често се користи као флуоресцентна ознака за аминокиселине или протеине.
Флуоресцентна резонанца Конверзија енергије (ФРЕТ) је корисна за студије ензима.Када се примењује ФРЕТ, полипептид супстрата обично садржи групу за обележавање флуоресценције и групу за гашење флуоресценције.Обележене флуоресцентне групе гаси се помоћу нефотонског преноса енергије.Када се пептид одвоји од дотичног ензима, група за обележавање емитује флуоресценцију.
10. Полипептиди кавеза
Кавезни пептиди имају оптички уклоњиве заштитне групе које штите пептид од везивања за рецептор.Када је изложен УВ зрачењу, пептид се активира, враћајући му афинитет према рецептору.Пошто се ова оптичка активација може контролисати у складу са временом, амплитудом или локацијом, пептиди кавеза се могу користити за проучавање реакција које се дешавају у ћелијама.Најчешће коришћене заштитне групе за кавезне полипептиде су 2-нитробензил групе и њихови деривати, који се могу увести у синтезу пептида преко заштитних деривата амино киселина.Деривати аминокиселина који су развијени су лизин, цистеин, серин и тирозин.Деривати аспартата и глутамата се, међутим, обично не користе због њихове подложности циклизацији током синтезе и дисоцијације пептида.
11. Полиантигени пептид (МАП)
Кратки пептиди обично нису имуни и морају бити повезани са протеинима носачима да би произвели антитела.Полиантигенски пептид (МАП) се састоји од више идентичних пептида повезаних са језгрима лизина, који могу специфично да експримирају имуногене високе потенције и могу се користити за припрему спојева протеина носача пептида.МАП полипептиди се могу синтетизовати синтезом у чврстој фази на МАП смоли.Међутим, непотпуно спајање резултира недостатком или скраћеним пептидним ланцима на неким гранама и стога не показује својства оригиналног МАП полипептида.Као алтернатива, пептиди се могу припремити и пречистити одвојено, а затим спојити са МАП.Пептидна секвенца везана за пептидно језгро је добро дефинисана и лако се карактерише масеном спектрометријом.
Закључак
Модификација пептида је важно средство за дизајнирање пептида.Хемијски модификовани пептиди могу не само да одржавају високу биолошку активност, већ и ефикасно избегавају недостатке имуногености и токсичности.У исто време, хемијска модификација може пептидима дати нека нова одлична својства.Последњих година брзо се развија метода активације ЦХ за постмодификацију полипептида и постигнути су многи важни резултати.
Време поста: 20. март 2023
